
Le cycle du fer joue un rŰle important dans la respiration :
- au niveau tissulaire , par l’hťmoglobine , qui assure le transport de l’oxygŤne molťculaire ,
- au niveau cellulaire , par les enzymes comportant du fer .
A - SCHEMA GENERAL DU CYCLE DU FER
1 - Les flux de fer sont ainsi schťmatisťs par Najean :

2 - Rťpartition du fer dans l’organisme
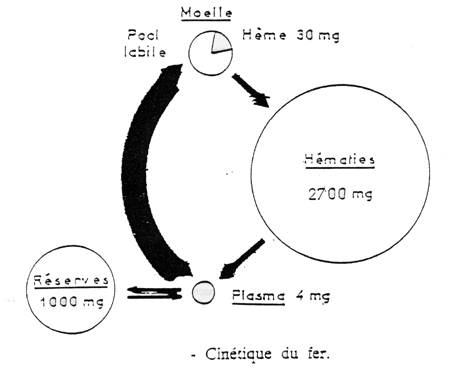
(tableau nį 63)
Il faut noter que les flux entre compartiments ne sont pas proportionnels au volume de ces compartiments en raison des vitesses trŤs diffťrentes de leurs taux respectifs de renouvellement .
(1 sur le schťma gťnťral)
1 - se fait sous deux formes :
sans parler du fer thťrapeutique ťventuel ;
2 - le contenu en fer des aliments est trŤs variable :
| mg / 100 mg | Mg / 1 000 Kcalories | |
| lait , beurre , fromages | 0,1 ŗ 0,3 | 0,3 ŗ 0,6 |
| carottes , choux , choux-fleurs , tomates | 0,5 ŗ 0,6 | 15 ŗ 25 |
| farine , pain , pois , haricots secs | 3,3 ŗ 7 | 13 ŗ 20 |
| fruits frais | 0,2 ŗ 0,7 | 3,5 ŗ 8 |
| chocolat | 3,1 | 5,4 |
| viandes | 2,3 ŗ 3,2 | 6 ŗ 25 |
| abats | 2,4 ŗ 15 | 7 ŗ 121 |
| huÓtres | 6 | 10,.7 |
| oeufs | 2,5 | 5,4 |
| poisson | 1 ŗ 2 | 7,5 ŗ 18 |
| boudin | 18 | 56,3 |
(le nourrisson nourri de lait et cťrťales est trŤs souvent carencť comme certains vieillards pour la mÍme raison)
3 - La quantitť de fer apportť par 1 000 kilocalories ingťrťes
est la mÍme sous toutes les latitudes (4 ŗ 12 mg par jour) ce qui veut dire que la carence martiale est parallŤle ŗ la malnutrition globale ; cependant besoins en fer et en calories ne sont pas toujours parallŤles , du bŻcheron suťdois ŗ l’enfant scolarisť ou la femme enceinte ŗ faible activitť physique !
4 - L’absorbabilitť du fer
- est trŤs variable selon les aliments dans lesquels il se trouve :
| fer non hťminique | fer hťminique | ||
| riz | 0 ŗ 2 % | soja | 6 ŗ 10 % |
| ťpinards | 1 ŗ 2 % | charcuterie | 10 ŗ 15 % |
| haricots | 2 ŗ 3 % | poisson | 10 ŗ 15 % |
| maÔs | 3 ŗ 4 % | foie | + de 20 % |
| laitue | 4 ŗ 5 % | muscle | + de 20 % |
TAUX D’ABSORPTION DU FER ALIMENTAIRE
(pour 2 ŗ 4mg de fer ingťrťs)
- Elle est meilleure pour le fer hťminique ŗ besoins et doses ťgaux que pour le fer non hťminique qui rentre dans des aliments moins coŻteux d’oý les carences martiales plus frťquentes dans les les milieux sociaux plus dťfavorisťs .
- Elle est modifiťe par la cuisson qui l’amťliore , la qualitť des rťcipients , en fer ou non , la prťsence d’argile qui la freine (eau boueuse des riziŤres ou pica des gťophages), la prise de thť ŗ table qui la freine , l’alcool , le vin surtout , qui l’accroissent en ťtant par ailleurs riches en fer .
(2 sur le schťma gťnťral)
est rťglťe pour faire face aux besoins , car il n’y a pas de rťgulation de l’excrťtion , mais cette rťgulation est mal connue .
1 - Le siŤge de l’absorption du fer
est essentiellement le duodťnum et la partie haute de l’ilťon , mais elle existe de moins en moins forte jusqu’au cŰlon ; certaines gastrectomies court-circuitent le duodťnum et entraÓnent une mal-absorption .
2 - Influence des facteurs externes :
- L’acide chlorhydrique de l’estomac dissout les complexes alimentaires et favorise la formation de chťlates avec le fer non hťminique .
- Dans l’intestin , les sťcrťtions intestinales , biliaires , pancrťatiques , libŤrent le fer des protťines alimentaires et abaissent le pH pour permettre sa liaison ŗ des chťlates ; l’importance de la motricitť intestinale est grande (mal-absorption des diarrhťes sťvŤres chroniques).
- Les habitudes alimentaires , par l’apport ťventuel de chťlateurs , accroissent l’absorption : biŤre d’Afrique du Sud ŗ base de maÔs et sorgho .
- La desferroxiamine B per os inhibe l’absorption , mais ne joue que sur le fer ionisť , d’oý son faible intťrÍt thťrapeutique .
3 - Influence des facteurs internes
Deux anťmies microcytaires carentielles gťnťtiques de la souris mk amŤnent ŗ ťvoquer deux ťtapes pour l’absorption du fer :
a. La fixation est un processus de liaison ŗ des rťcepteurs " transferrine-like " de la bordure en brosse des cellules muqueuses duodťnales , liť aux besoins en fer , fixant le fer hťminique tel quel , dťtachant de ses chťlates le fer non hťminique .
b. Le fer pťnťtrant dans les cellules muqueuses
- a trois destinťes possibles :
- Dans la muqueuse intestinale , le fer hťminique est libťrť du cycle porphyrinique par la xanthine-oxydase ; la protťine de transfert intracellulaire est une transferrine , identique ou similaire ŗ celle du plasma .
4 - Rťgulation physiologique de l’absorption du fer :
a. elle serait liťe au rapport quantitatif entre les trois voies possibles , par l’intermťdiaire de la saturation variable de la transferrine cellulaire intestinale , c’est le classique " bloc muqueux ".
b. Mais cette rťgulation n’est pas parfaite :
pas de rťgulation pour le fer ionisť (accident d’intoxication possible chez l’enfant), excŤs de fer apportť chez l’alcoolique , hyperabsorption des dysťrythropoÔŤses chroniques (thalassťmies , anťmies sidťroblastiques), hťmochromatose gťnťtique .
5 - Moyens d’ťtude de l’absorption du fer
On n’utilise plus que les mťthodes isotopiques :
a. Le radiofer
- est administrť sous forme de 59Fe ferreux per os ŗ jeun en dose traceuse , ou d’aliments marquťs " in vivo " ce qui est trŤs lourd , ou encore de repas marquť par " extrinsic tag " , repas additionnť d’un peu de radiofer .
- Trois mťthodes sont valables et prťcises :
la comparaison de la dose absorbťe avec celle ťliminťe , la comparaison de l’incorporation " in vivo " dans les hťmaties de deux radiofers donnťs l’un per os , l’autre par voie veineuse , ce qui est trŤs long et coŻteux , le comptage global dŤs aprŤs l’ingestion du repas marquť et aprŤs 8 jours (fin du transit intestinal) ce qui est lourd et coŻteux aussi .
- Les comitťs d’ťthique , vue la petite dose de radio-activitť ingťrťe , acceptent leur utilisation mÍme chez le jeune enfant ou la femme enceinte ou chez les volontaires sains .
- Trois objectifs sont en effet possibles :
b. Un test au radiocobalt puisque l’absorption du cobalt suit celle du fer , est possible en quelques heures , basť sur le recueil des urines pendant 6 heures aprŤs ingestion d’une dose traÁante .
La dťficience en fer est un problŤme de santť publique : concernant 20 ŗ 30 % des sujets dans les pays pauvres et une frange de la population dans les pays industrialisťs .
Le dťpistage s’appuye essentiellement sur la mesure de la ferritinťmie .
La " fortification " systťmatique de l’alimentation est rťservťe aux pays oý la carence est habituelle et l’anťmie frťquente en incorporant le fer ŗ un aliment largement consommť , ne changeant pas de goŻt , si le prix n’en est pas trop accru etc .... (farine , riz , sucre , condiments , farines pour jeunes enfants).
E - TRANSPORT DU FER DANS LE PLASMA ET PROTEINES PORTEUSES DE FER
1 - La transferrine , ou sidťrophiline est la forme exclusive de transport de fer dans le plasma .
a. C’est une glycoprotťine de 679 rťsidus d’acides aminťs et 76 000 daltons de poids molťculaire qui possŤde 28 phťnotypes permettant de dťfinir 28 groupes sťriques , qui peut fixer 2 atomes de fer ferrique ; on la dosait par sa capacitť ŗ fixer le fer , mais ce " fer sťrique " a perdu beaucoup de son intťrÍt pratique car il varie du simple au double dans le nycthťmŤre .
b. Sa synthŤse est hťpatique , surtout , avec un renouvellement de 15 % par jour , non modifiťe par les besoins .
c. Seule cette transferrine peut dťlivrer le fer ŗ la cellule rouge jeune (3 sur le schťma gťnťral):
l’a-transferrinťmie congťnitale est rapidement mortelle et le fer libre circulant aprŤs intoxication est toxique (risque de collapsus).
d. Seules certaines cellules peuvent fixer la molťcule de transferrine porteuse de fer:
- ce sont : les cellules du placenta , les hťpatocytes , mais surtout les cellules rouges jeunes :
4 fois plus pour l’ťrythroblaste basophile que pour le rťticulocyte , mais ce n’est plus possible pour le globule rouge mŻr .
- Ces cellules possŤdent des rťcepteurs dont on connaÓt bien la biologie molťculaire ;
- la fixation dure 10 ŗ 30 minutes avec fixation du complexe Fe-Tf au rťcepteur , internalisation , libťration du fer dans la cellule , ŗ bas pH , libťration de la transferrine libre et reconstitution du rťcepteur .
- La richesse en rťcepteurs intervient :
ils sont un marqueur de diffťrenciation de la lignťe rouge et on les reconnaÓt par un anticorps monoclonal comme OKT-9 .
2 - La ferritine
- est une coque protťique comportant un coeur de fer de taille variable et comportant 24 sous-unitťs basiques et acides ŗ rťpartition variable .
- Le fer ferreux s’y accumule , s’y oxyde , et peut en ressortir gr‚ce ŗ des flavines rťduites . Au delŗ de 4 000 atomes de fer par molťcule , on aboutit ŗ l’hťmosidťrine , visible en coloration de Perls .
- La ferritine du plasma , sťcrťtťe par l’hťpatocyte , prťsente au taux de 12 ŗ 300 ng / ml (ou Ķg/l) , ne transporte pas de fer , mais les variations de son taux sont parallŤles ŗ celles des rťserves de fer de l’organisme entier , d’oý le grand intťrÍt de son dosage .
3 - La lactoferrine
glycoprotťine voisine de la ferritine , est surtout prťsente dans le lait et sert ŗ l’apport de fer au nourrisson .
F - UTILISATION DU FER PAR L’HEMOGLOBINOSYNTHESE
(4 sur le schťma gťnťral)
1 - Apport du fer aux ťrythroblastes
a. La traversťe de la membrane suppose donc un rťcepteur capable de recevoir le fer dťtachť de la transferrine ; sa rťgulation n’est pas connue mais n’est absorbť que le fer utile ŗ la biosynthŤse et seulement par les ťrythroblastes jeunes .
b. Le passage de la membrane ŗ la mitochondrie est trŤs rapide (moins de 30 minutes) gr‚ce ŗ une protťine " transferrine-like " diffťrente de celle plasmatique .
c. Les inducteurs comme l’ťrythropoÔťtine n’agissent pas directement sur le taux des rťcepteurs ou la vitesse de transfert , mais les augmentent indirectement par action directe sur l’hťmoglobino-synthŤse en induisant la transcription des mARN de chaÓnes globiniques .
2 - L’incorporation du fer ŗ l’hŤme a lieu dans les mitochondries gr‚ce ŗ l’hŤme-synthťtase ou ferro-chťlatase; un " dťficit " ŗ ce niveau engendre l’accumulation de fer sous forme de ferritine , puis hťmosidťrine dans les ťrythroblastes les plus mŻrs prenant le nom de " sidťroblastes " , pathologiques ici ; la toxicitť locale du fer donne un avortement mťdullaire et son recyclage , associť aux transfusions, une hťmochromatose ; normalement , il n’y a que peu de fer dans les ťrythroblastes : 10 % de sidťroblastes de type I ŗ un ou deux petits grains de fer qui sont des ťrythroblastes trŤs peu mŻrs .
3 - Moyens d’ťtude
4 - Transfert aux autres organes
la fixation hťpatique peut intťresser les hťpatocytes et les cellules de KŁppfer , la fixation placentaire , 300 mg par grossesse , se fait gr‚ce ŗ la prťsence de rťcepteurs sur les villositťs placentaires contre un gradient de concentration .
G - LE FER DE L’HEMOGLOBINE CIRCULANTE
(5 sur le schťma gťnťral)
- reprťsente 70 % du fer total de l’organisme (prŤs de 3 grammes chez l’adulte);
- chaque gramme d’hťmoglobine comporte 3,4 mg de fer et un litre de sang ŗ peu prŤs 500 mg : l’apport transfusionnel dans les hťmolyses chroniques (sans perte de fer) comporte un risque d’hťmochromatose , les hťmorragies , digestives et gťnitales , engendrent une dťperdition de fer ;

(schťma nį 63)
- la ferrimťtrie permet un dosage trŤs prťcis de l’hťmoglobine en solution ;
- le fer hťmoglobinique est bivalent Fe++ , son oxydation en Fe+++ (mťt-hťmoglobinisation) rend l’hťmoglobine impropre au transport de l’oxygŤne ; il a du fait de sa structure ťlectronique pťriphťrique
4 liaisons de coordination avec les 4 noyaux pyrrole de l’hŤme ,
2 liaisons de coordination avec des histidines globiniques sises en F8 et E7 et la fixation rťversible d’oxygŤne en E7 maintient l’ťtat ferreux dans les conditions normales .
H - PERTES (et besoins) EN FER EXOGENE
(5 bis sur le schťma gťnťral)
1 - Pertes communes aux deux sexes (trŤs faibles normalement)
a. Pertes fťcales (0,4 ŗ 0,5 mg / jour chez l’adulte)
b. Pertes urinaires (0,1 mg / jour chez l’adulte)
on peut accroÓtre cette ťlimination par la desferroxiamine B intraveineuse qui chťlate le fer .
c. Pertes cutanťes (1 ŗ 5 Ķg / jour)
d. Don du sang trop frťquent , surtout si le sang est payť !
2 - Pertes propres ŗ la femme
a. La menstruation ťlimine 40 ŗ 50 ml de sang par cycle , soit 20 ŗ 25 mg de fer (davantage sous stťrilet , moins sous contraception orale), ce qui fait 0,8 mg de fer / jour sur l’ensemble du cycle , mais parfois plus de 1 mg chez 10 % des femmes considťrťes comme normales .
Les apports seront donc ŗ multiplier par 2 ou 4 par rapport ŗ l’homme .
Les hťmorragies gynťcologiques sont la cause la plus frťquente des anťmies hypochromes ferriprives de la femme en pťriode d’activitť gťnitale , car si la menstruation dťpasse 80 ml , les rťserves risquent de s’ťpuiser .
b. La grossesse
Il y a perte supplťmentaire de fer :
Par contre , l’arrÍt des rŤgles compense en faible part ce dťficit .
Globalement , les besoins en fer augmentent progressivement pendant la grossesse jusqu’ŗ 4 mg / jour , comme aussi le coťfficient d’absorption du fer , et faute d’apport complťmentaire , il y aura ťpuisement des rťserves de fer .
Les anťmies de la grossesse , le plus souvent ferriprives , surtout dans nos contrťes , sont liťes ŗ des grossesses rťpťtťes chez les sujets ŗ la limite de la carence (ťmigrťes) et certains prťconisent une supplťmentation systťmatique ; le retentissement sur l’enfant est nul tant sur le plan obstťtrical que sur le plan martial .
3 - La croissance correspond ŗ une augmentation des besoins pour accroÓtre le capital martial et ceci va requťrir un supplťment de 0,5 mg / jour .
Le foetus a rťcupťrť le fer maternel en fin de grossesse pour le stocker dans son foie , mais le prťmaturť est plus exposť aux carences ; le fer de la polyglobulie nťonatale est rťcupťrť .
Les besoins sont importants ŗ deux moments : dans le second semestre de la vie et ŗ la pubertť , pťriodes oý sont frťquentes les anťmies hypochromes , surtout si le rťgime est mal ťquilibrť et certains prťconisent lŗ aussi une supplťmentation systťmatique (cťrťales avec fer incorporť).

(schťma nį 64)
4 - La recherche d’un excŤs de pertes de fer
- repose en pratique
sur un interrogatoire dťtaillť : pertes digestives , hťmorroÔdes , rŤgles (durťe , consommation de garnitures) , autres hťmorragies comme des ťpistaxis , don du sang ..... et un examen clinique soigneux ,
- car le marquage des hťmaties in vitro , au 59Fe , suivi de la mesure de la radio-activitť corporelle totale ou dans les excreta , est une mťthode trŤs prťcise , mais inapplicable en routine .
5 - La thťrapeutique martiale
a. doit toujours reposer sur le fer oral :
sels ferreux , fonction de la tolťrance gastrique (glutamate , fumarate ...), avec des additifs facilitant l’absorption (manitol) et de l’acide ascorbique , alors que la vitamine B 12 n’apporte qu’un surcoŻt inutile ; il faut savoir que le fer oral colore les selles !
b. Le fer parentťral intramusculaire , longtemps interdit en France , n’a que d’exceptionnelles indications .
c. Des accidents toxiques aigus sont possibles chez l’enfant aprŤs prise accidentelle d’une dose majeure.
I - MECANISMES DE REUTILISATION DU FER
(6 sur le schťma gťnťral)
1 - L’ťrythrophagocytose des hťmaties vieillies par les macrophages , mťdullaires essentiellement , est suivie d’une libťration du fer dans ces macrophages , sans ťlimination , ni stockage ŗ long terme , en physiologie ; dans les anťmies hťmolytiques , il en va de mÍme avec une destruction splťnique ou hťpato-splťnique .
2 - Le fer libťrť est pour plus de 50 % recyclť en quelques heures ŗ travers la transferrine plasmatique qui le ramŤne aux ťrythroblastes mťdullaires ; le reste est incorporť aux rťserves ŗ renouvellement lent , c’est ŗ dire en ferritine .
En pathologie , le recyclage est rapide en cas de carence , mais en cas de lourd excŤs , la ferritine est transformťe en hťmosidťrine .
3 - Les moyens d’ťtude de la rťutilisation nťcessitant un double marquage de la transferrine et de globules rouges lťsťs , sont trŤs complexes .
4 - Deux troubles existent ŗ ce niveau :
- la captation du fer dans les rťserves lentement rťutilisables , lors des infections sťvŤres chroniques , maladies inflammatoires graves maladies malignes , rťversible lors de la cure si elle est possible de la maladie en cause , ou sous simple traitement anti-inflammatoire , est source d’anťmies hypochromes hyposidťrťmiques non ferriprives , trŤs frťquentes , ŗ fer sťrique bas , mais ŗ ferritinťmie ťlevťe .
- Les hťmorragies viscťrales intratumorales et l’hťmosidťrose pulmonaire idiopathique .
(7 sur le schťma gťnťral)
1 - Donnťes physiologiques :
- le fer arrive du plasma , et parfois de l’apport alimentaire , de la destruction des hťmaties dans les macrophages , surtout .
- Il est restituť ŗ la transferrine plasmatique pour Ítre livrť aux ťrythroblastes , aprŤs rťduction par la ferriductase et les flavines rťduites .
- Le stockage est surtout hťpatique (plus du tiers): cellules de KŁppfer , mais aussi hťpatocytes , plus accessoire est le stockage splťnique et mťdullaire (un tiers) ou musculaire (un tiers) .
2 - Donnťes biochimiques : la forme de stockage est la ferritine .
- Les ferritines hťpato-splťniques formes de rťserve , se diffťrencient de celles placentaires , musculaires , tumorales , par le pourcentage ťlevť de subunitťs L basiques .
- La synthŤse d’apoferritine , protťine non chargťe de fer , est le fait surtout des hťpatocytes , induite par la quantitť de fer du milieu.
- Plus elle est chargťe en fer ferrique , ce qui peut porter son poids molťculaire de 480 000 daltons environ ŗ prŤs de 900 000 , moins elle est soluble et apte ŗ rendre son fer ; ŗ la limite se forme l’hťmosidťrine , totalement insoluble , inapte ŗ rendre le fer , vťritable corps ťtranger ŗ l’organisme .
3 - Donnťes morphologiques :
a. la ferritine est visible en microscopie ťlectronique , d’aspect polygonal ;
b. L’hťmosidťrine sorte de polymŤre de ferritine englobant des lipides , glucides , protťines , est le " pigment ocre " des histologistes , colorable au Perls , en grains visibles en microscopie optique .
4 - L’ťvaluation des rťserves martiales
- fait classiquement appel au Perls sur biopsies hťpatiques ou sur ponction et biopsie mťdullaire en ne tenant compte que du fer des macrophages ;
- la ferritinťmie , bien que la ferritine plasmatique n’ait aucun rŰle dans le transport du fer , est un excellent reflet des rťserves martiales, et elle est devenue facile ŗ doser par immuno-enzymologie .
- Le test au DesfťralR est un test dynamique permettant de prťsumer d’une efficacitť thťrapeutique .
5 - La limitation des surcharges martiales consiste ŗ diminuer les apports et surtout ŗ augmenter les pertes dans les hťmochromatoses par des saignťes ou par des chťlateurs en cas d’hťmopathies diverses exigeant des transfusions rťpťtťes .

(schťma nį 65)
1 - La myoglobine a une teneur en fer identique ŗ l’hťmoglobine , 2 ŗ 3 mg de fer par gramme de muscle , d’oý l’intťrÍt dans l’apport alimentaire de la viande qui contient aussi du sang .
2 - Le fer enzymatique peu abondant , mais essentiel aux mťtabolismes , est soit dans un groupement hťminique (catalases) soit non hťminique dans les flavoprotťines .
Tout ceci montre bien l’importance du fer en hťmatologie :
tout bilan d’une anťmie hypochrome doit comporter son exploration , non plus par le dosage du fer sťrique , dťpassť , mais par celui de la ferritinťmie , avant que les cartes ne soient brouillťes par une thťrapeutique martiale intempestive , trop frťquement observťe , voire associťe ŗ d’autres produits inutiles (B 1 , B 6 , B 12 etc....) .
| Commentaires et Questions |